Ziekte van Alzheimer – p-Tau217 als nieuwe biomarker


De diagnostiek van Alzheimer evolueert snel. Nieuwe therapieën maken tijdige detectie steeds belangrijker. Plasmabiomarkers kunnen hieraan voldoen en maken het mogelijk de ziekte minder invasief op te sporen. Ze dienen echter niet als screeningtest aangewend te worden en hebben enkel zin bij patiënten met een hoge pretestprobabiliteit. Deze tekst bespreekt de ziekte van Alzheimer en de meest belovende van deze biomarkers: p-Tau217.
Inleiding
Wereldwijd lijden meer dan 57 miljoen mensen aan dementie, waarvan naar schatting 220.000 mensen in België. Het merendeel van deze gevallen betreft seniele dementie van het Alzheimer type, goed voor meer dan 70% van de diagnoses. Andere vormen van dementie zijn vasculaire dementie, Parkinsondementie, Lewy body-dementie en frontotemporale dementie. Dementie is wereldwijd de zevende belangrijkste doodsoorzaak en behoort tot de hoofdoorzaken van invaliditeit bij ouderen.
In België werd het in 2019 volgens Sciensano zelfs als de belangrijkste doodsoorzaak beschouwd. Preventie is mogelijk door leefstijlaanpassingen waarbij gesteld kan worden dat elke vorm van cardiovasculaire preventie tevens een beschermend effect heeft tegen cognitief deficit. Ook zijn er recent ernstige aanwijzingen dat vaccinatie met recombinant varicella-zostervaccin een sterke risicoreductie met zich mee kan brengen.
Eén van de grootste uitdagingen voor artsen blijft het tijdig identificeren van personen met de ziekte van Alzheimer. Het opsporen van milde cognitieve achteruitgang biedt de mogelijkheid om in een vroeg stadium in te grijpen en de progressie van Alzheimer af te remmen.
Tot heden zijn de testen (total-tau, p-tau en amyloid-beta) op cerebrospinaal vocht (CSV) en positron emission tomography (amyloid-beta-PET en Tau-PET) de gouden standaard voor de diagnose. Het zijn enerzijds invasieve (CSV) en anderzijds beperkt beschikbare en dure (PET) onderzoeken, die helaas vaak uitgesteld worden met mogelijk latere diagnose tot gevolg. De komst van plasmabiomarkers kan daar verandering in brengen.

Pathogenese
Tot heden zijn de testen (total-tau, p-tau en amyloid-beta) op cerebrospinaal vocht (CSV) en positron emission tomography (amyloid-beta-PET en Tau-PET) de gouden standaard voor de diagnose. Het zijn enerzijds invasieve (CSV) en anderzijds beperkt beschikbare en dure (PET) onderzoeken, die helaas vaak uitgesteld worden met mogelijk latere diagnose tot gevolg. De komst van plasmabiomarkers kan daar verandering in brengen.
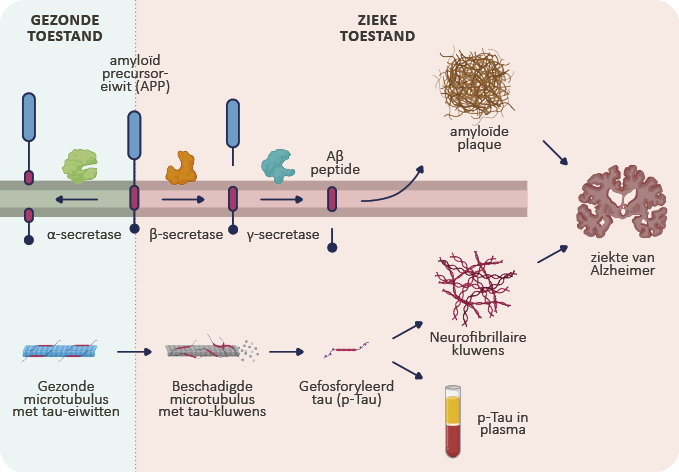
Tau (tubuline-geassocieerde unit) stabiliseert normaal gesproken de microtubuli in de hersencellen en maakt intracellulair transport van voedingsstoffen mogelijk. Bij (hyper)fosforylatie wordt de binding van Tau met de microtubuli sterk bemoeilijkt, wat op termijn resulteert in de vorming van aggregaten en neurofibrillaire kluwen (NFT) in de neuronen.
Uiteindelijk leidt dit tot massale neuronale sterfte, verlies van synapsverbindingen, cerebrale atrofie met afname van de corticale gebieden en het vergroten van de ventrikels en de corticale sulci.
Deze neurodegeneratie in de hersenen ontstaat jaren vóór het verschijnen van de klinische symptomen, mogelijk zelfs 15 à 20 jaar voorafgaand aan de cognitieve achteruitgang.

Klinische symptomen
Progressieve neurodegeneratie leidt initieel tot een stadium van mild cognitive impairment (MCI), dat in een deel van de patiënten overgaat naar klinisch manifeste Alzheimer dementie. Geheugenverlies, verminderde korte-termijn geheugenfunctie, veranderingen in gedrag, verstoorde spraak, problemen met uitvoerende functies, afname van sociale activiteiten en moeite met zelfstandig functioneren zijn veel voorkomende symptomen van beginnende dementie. Daarnaast kunnen psychische tekenen zoals hallucinaties, agressief gedrag, excessieve activiteit, depressie en minder specifieke symptomen zoals loopstoornissen en verwardheid ook wijzen op beginnende dementie.
Bij het vermoeden van cognitieve achteruitgang of dementie kan de MMSE (Mini-Mental State Examination) worden afgenomen als screeningsmaat voor het cognitief functioneren.
De vragenlijst evalueert meerdere cognitieve domeinen waaronder aandacht en rekenen, oriëntatie in tijd en ruimte, geheugen, uitgestelde herinnering, taalvaardigheid en praxis.
Lage totaalscore wijst op ernstigere cognitieve stoornissen. Een afkapwaarde < 25 wordt meestal gebruikt als indicatie voor een mogelijke cognitieve stoornis.
Genetische aanleg
Ongeveer 10% van de patiënten met AD heeft te maken met de early-onset Alzheimer’s disease (EOAD), of jongdementie. 15% van deze gevallen zijn erfelijk. EOAD vertoont dezelfde symptomen als late-onset Alzheimer maar de ziekte begint vóór de leeftijd van 65 jaar.
De late-onset variant van de ziekte van Alzheimer is in de minderheid van de gevallen genetisch gelinkt met het APOE-gen. In dit kader van AD is ApoE-ε4 homozygotie belangrijk. Het dragerschap kan opgespoord worden met een eenvoudige immunologische test ter bepaling van E4 (serum). Bij positiviteit dringt een verdere genotypering zich op.
Ongeveer 15% van de Belgische bevolking is heterozygoot voor het ε4-allel, terwijl 1-5% homozygoot ε4/ε4 is. Laatst genoemde genotype geeft 60% kans op het ontwikkelen van AD. In november 2024 keurde het EMA het gebruik van Leqembi® (Lecanemab) goed voor behandeling in de vroege stadia van Alzheimer, op voorwaarde dat de patiënt niet homozygoot ε4/ε4 is. Patiënten hebben in dit geval een verhoogd risico op ernstige bijwerkingen, zoals oedeem en bloedingen in de hersenen.

Biomarkers in bloed (plasma)
Recent kwamen er verschillende plasma biomarkers beschikbaar die amyloid pathologie kunnen aantonen in het bloed, waaronder p-Tau (181 en 217), de ratio Aβ42/Aβ40, NFL (neurofilament-light peptide) en GFAP (glial fibrillary acidic).
De meest veelbelovende is p-Tau217, een hypergefosforyleerd Tau-eiwit dat specifieker is voor de ziekte van Alzheimer dan p-Tau181. Deze biomarker wordt bepaald op EDTA-plasma.
p-Tau217 dient selectief te worden aangevraagd, enkel bij patiënten met een hoge pretestprobabiliteit (klinisch vastgestelde MCI of MMSE > 20 / < 25). Een zorgvuldige patiëntenselectie is essentieel om de diagnostische waarde te maximaliseren en onnodige onderzoeken of foutieve behandelingen te vermijden. Bij patiënten met een lage baselinekans op Alzheimer of aspecifieke klachten is het risico op fout-positieve resultaten groter, wat kan leiden tot detectie van klinisch irrelevante amyloïdpathologie en onnodige interventies.

Interpretatie
Two cut-off approach
Voor de interpretatie van deze marker wordt een two cut-off approach gehanteerd. Dit verhoogt de performantie van de test aanzienlijk (sensitiviteit en specificiteit zijn > 95%). Een waarde onder de eerste cut-off (p-Tau217 < 0,28 pg/mL) kan beschouwd worden als rule-out. Een waarde boven de tweede cut-off (p-Tau217 > 0,50 pg/mL) heeft een hoge specificiteit (> 95%) voor onderliggende Alzheimer pathologie bij personen met cognitieve stoornissen. De grijze (intermediate) zone tussen de twee cut-off waarden (0,28 – 0,50 pg/mL) wordt aanvullend onderzoek aanbevolen om Alzheimer pathologie te bevestigen of uit te sluiten (CSV-analyse of PET).
Aandacht bij verlaagde nierfunctie
Bij de interpretatie van p-Tau217 concentraties dient rekening gehouden te worden met de nierfunctie. Studies tonen aan dat patiënten met een verminderde glomerulaire filtratiesnelheid (eGFR < 60 mL/min/1,73 m²) verhoogde plasmawaarden van p-Tau217 kunnen vertonen. De verminderde renale klaring van tau-eiwitten kan inderdaad leiden tot een vals-verhoogde p-Tau217 waarde, maar zal zelden aanleiding geven tot een rule in resultaat. Voor eGFR < 45 mL/min/1,73 m² is de probabiliteit iets hoger en dient bij verhoogde waarden de nodige voorzichtigheid in acht genomen te worden.

Take away message
- Geen algemene screeningstest
- p-Tau217 NIET aanvragen bij een patiënt:
- Zonder symptomen
- Met symptomen maar MMSE > 24
- Met symptomen maar neuropsychologisch onderzoek niet indicatief voor Alzheimer
- Bloedafname op EDTA. Bewaren in de koelkast (2-8°C).
Bezorg het staal binnen de 24u na afname aan het labo. - Two cut-off approach
- < 0,28 pg/mL = Rule out (negatief)
- 0,28 pg/mL – 0,50 pg/mL = Intermediate (grey zone) → CSV/PET
- > 0,50 pg/mL = Rule in (positief) → diagnostisch
Referenties
- World Health Organization – fact sheets dementia
- Elecsys Phospho-Tau (217P) Plasma. Method Sheet. Roche Diagnostics (2025)
- Exploring kidney function threshold for plasma p-Tau 217 use. Alzheimer’s dement. 2025; 21 (suppl 2); e105379.
- Jack CR, Andrews JS, Beach TG, Buracchio T, Dunn B, Graf A, et al. Revised criteria for diagnosis and staging of Alzheimer’s disease: Alzheimer’s Association Workgroup. Alzheimer’s & Dementia. 2024;20(8):5143-69
- Roth S, Burnie N, Suridjan I, Yan JT, Carboni M. Current Diagnostic Pathways for Alzheimer’s Disease: A Cross-Sectional Real-World Study Across Six Countries. J Alzheimers Dis Rep. 2023;7(1):659-74
- https://meetinstrumentenzorg.nl/instrumenten/mini-mental-state-examination-gestandaardiseerde-versie/
